
こんにちは、ノブです。
こちらは創薬(wet)Advent Calendar 2019の15日目の記事です。
久しぶりに創薬関係の話を。今回はモダリティと薬価について全3回に分けて考えてみました。第1回目の本日は「モダリティ」という概念について。 薬作りに興味がある方や、創薬研究者になりたての方への前提知識、という内容です。非常に広範な話になるため、詳細な説明は各リンク先に任せます。 知っている項目は読み飛ばしてください。
モダリティとは
10年くらい前までは「鍵と鍵穴の原理以外のMOA(mode of action)で使用するもの」程度の使われ方をしていたような気がします。PETとか放射性治療薬とかですね。ただ、最近では薬として用いられる化合物の分子種を区別するための用語になりました。
各種分子種を紹介してくれている製薬企業のウェブサイトがありますので、 ご興味がある方は以下をご参照ください。低分子、マクロサイクル、抗体、ナノボディ、ADC、ペプチド、核酸医薬、ワクチン、細胞治療、AAVなど、多岐にわたっております。
①Amgen Science: The Shape of Drugs to Come
②AstraZeneca: Drug modalities
薬の作用機序とモダリティ
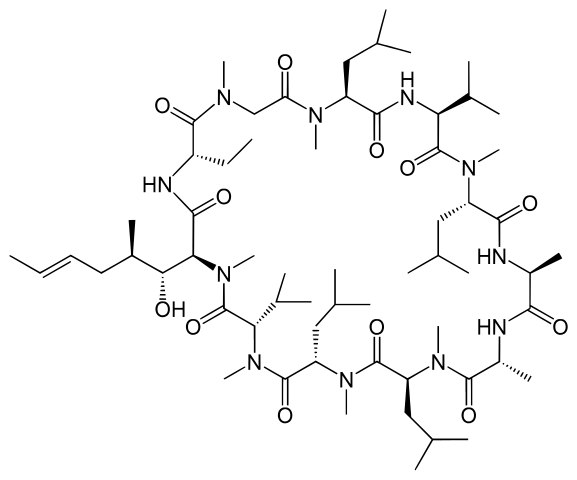
10年前までは化学者が触っている薬といえば、そのほとんどが低分子化合物(本記事では「分子量500以下の分子」と定義します)でした。例外は天然物化合物そのもの or その誘導体の中分子(分子量が500~2000)くらいでしょうか。(例:シクロスポリン、分子量:1202.61。下図参照。デカい。)
2000年代初頭までは薬の作用機序といえば「鍵と鍵穴の関係」で説明されていました。(もちろん、アロステリックなどの考え方もありましたが。)標的となるタンパクのくぼみに薬の分子が良い感じでハマり、タンパク独自の働きを活性化 or 阻害することで薬効が発現する。というフワッとした説明だったのです。(下図)
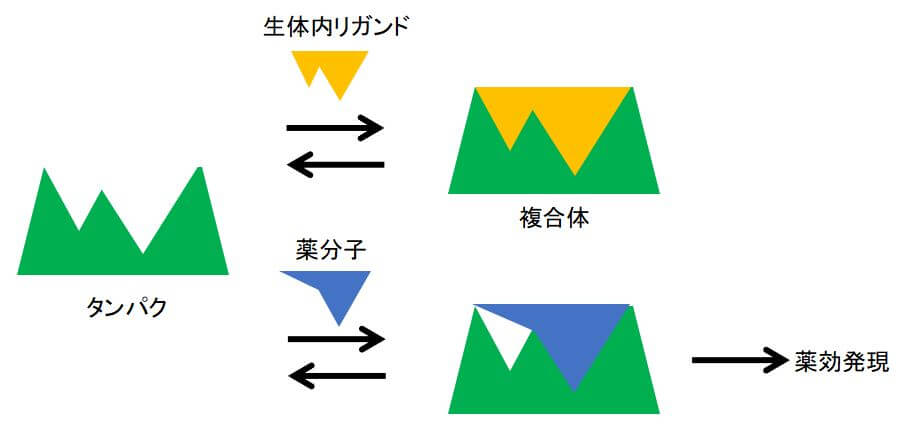
バイオロジーが発展して一番の変化は「疾患発症の様々なメカニズムが明らかになったこと」です。 タンパク同士の相互作用が解明されたり、タンパク情報の元となるDNAやRNAが“どのように生体内で制御されているか”という理解が深まったりで話は複雑化しました。
そしてその中には、既存の低分子では狙うことが難しいターゲットが数多くありました。そうなると異なるモダリティが必要となります。ターゲットの作用点の構造や作用メカニズムが分かっている場合は対応する分子も設計しやすくなります。このような経緯で様々なモダリティが生み出されました。
また、ケミカルバイオロジー分野の発展とともにヒット化合物を検出する手法や結合状態を評価する手法が発達したことも種々のモダリティを生み出す要因となりました。
具体的にはファージディスプレイ、DELなどのライブラリ構築&検出法や、SPR、ITC、NMR、ASMS、DSCなどの結合状態評価法です。(この辺をだいたい説明できればメドケム初心者レベルはクリアではないでしょうか。)
特にケミストに大きな衝撃を与えたのはタンパク-タンパク結合(PPI: protein-protein interaction)阻害剤だと思います。タンパク間の相互作用は広く浅い接合面で行われていることが多いため、表面積が小さい低分子ではその作用を阻害することが難しいとされていました。
そこに登場したのがalpha helix mimeticsという分子。十分にデザイン可能な低分子~中分子でタンパク間の相互作用をブロックします。
上記の発見や技術進歩のおかげで、タンパクが生体内でどんな相手とどのように結合しているか、その結果何が起こっているかを今まで以上に詳細に意識する必要が出てきました。
つまり、生体内のメカニズムベースで疾患治療を考えながら、どのモダリティが良いか選択しなければなりません。ケミストが有機合成だけ分かっていれば良い時代は完全に終わったのです。
現在は他にも、生体内の分解機構を利用してターゲットタンパクを分解してしまうPROTAC(proteolysis-targeting chimeric molecules)やAUTAC(Autophagy-targeting chimera)、RNAのスプライシングプロセスをコントロールするSplicing modulator、CRIAPRの技術を用いて遺伝子発現量を上昇させる化合物まで開発されつつあります。この20年で「鍵と鍵穴の関係」では収まりがつかなくなるくらい創薬科学は進歩しました。
さらには脂肪鎖やPEGによる修飾、リポソームに封入された分子を用いることで、体内での安定性や細胞膜透過性の向上、ターゲットへの送達を志向した技術も発展しました。
というのが低分子~中分子だけの話です。ADC(antibody-drug condugate)のような異なるモダリティを組み合わせた薬剤もありますし、そもそも2つの機能を有しているPROTACをさらに抗体とくっつけたPAC (PROTAC-antibody condugate) という分子も生まれ、試薬として販売までされていたりします。また、他のモダリティを低分子に置き換える試みもさかんに進んでいます。訳わからんですね。わからなくなってきたのでとりあえず本日はこのへんで。
ノブ
※より詳しい話を知りたい方へ。以下の論文が参考になりました。
・New Modalities, Technologies, and Partnerships in Probe and Lead Generation: Enabling a Mode-of-Action Centric Paradigm
・New Modalities for Challenging Targets in Drug Discovery
・Emerging modes-of-action in drug discovery)

コメントはまだありません